Elementlerin Elektron Alma - Verme Ve Ortaklaşma Eğilimleri
ELEMENTLERİN ELEKTRON ALMA - VERME VE ORTAKLAŞMA EĞİLİMLERİ
İyonik bileşikler oluşurken metal elektron verir ametal ise elektron alır. Ancak hem metaller hem de ametaller soy gazlarla bileşik oluşturamazlar bu durum elektron dizilimi ile ilgilidir.
Atomlar kararlı hale gelmek için son yörüngelerindeki elektronlarını soy gaz elektron düzenine benzetirler.
Bir atomun son yörüngesindeki elektronunu ikiye tamamlayarak He soy gazına benzemesi olayına Dublet kuralı sekize tamamlayarak He dışındaki soy gazlara benzetmesi olayına ise Oktet kuralı denir.
Katman elektron dizilimi için iki kural vardır. Elektronlar katmanlara yerleşirken 2n2 kuralına göre yerleşir. Elektronlar katmanlara yerleşirken en düşük enerjiliden yüksek enerjiliye doğru yerleşirler. Yani düşük enerjili katmanlar dolmadan yüksek enerjili katmanlara elektron yerleşemez.
Elementlerin artan atom numaralarına göre yan yana getirilmesi ile oluşturulan yatay sıralara periyot denir. Her elementin bulunduğu periyot numarası kadar katmanı vardır. Bir elementin en son enerji katmanındaki elektronlarına değerlik elektronları denir.
Kimyasal özellikleri birbirine benzeyen elementler alt alta getirilerek sütunları oluştururlar.
Bu sütunlara gurup denir. 8 tane "A" gurubu ve 8 tane "B" grubu vardır.
Atom çekirdek ve çekirdeğin etrafında oluşan enerji katmanlarından meydana gelmiştir. Bu enerji katmanları bulundurdukları elektron sayılarına göre; 2-8-8-18-18-32-32şeklinde sıralanırlar.
Örnek: Aşağıdaki atomların enerji katmanlarınıyazınız? (1H, 5B, 6C, 8O, 11Na, 20Ca,)
Aynı periyot elementlerinin yörünge sayıları aynı olup atom çapları, atom hacimleri, elektron verme eğilimleri,fiziksel ve kimyasal özellikleri farklıdır.
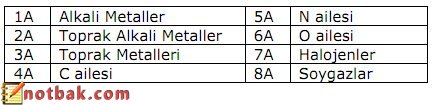
Periyodik cetvelde grupların özel adları vardır. Bunlar;
Not: Bir atomun en yüksek enerji seviyesindeki elektronlarına değerlik elektronları denir. A grubu elementlerinin grup numaraları ile değerlik elektron sayıları birbirine eşittir.
A gurubu elementlerinin alabileceği maksimum ve minimum değerlikler tablodaki gibidir.
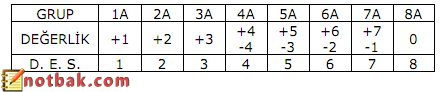
Örnek: Aşağıdaki atomların enerji katmanlarını yaza- rak grup numaralarını ve değerlik elektron sayılarını bulunuz? (5B, 7N, 1H, 6C, 8O, 11Na, 20Ca)
Ekleyen : notbak.com